

 公司总机
公司总机 贵宾直线
贵宾直线 公司地址
公司地址北京市丰台区南方庄1号院
安富大厦511室
1、商务部 海关总署 国家药品监督管理局公告2020年第5号《关于有序开展医疗物资出口的公告》
自4月1日起,出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的企业向海关报关时,须提供书面或电子声明,承诺出口产品已取得我国医疗器械产品注册证书,符合进口国(地区)的质量标准要求。海关凭药品监督管理部门批准的医疗器械产品注册证书验放。上述医疗物资出口质量监管措施将视疫情发展情况动态调整。
2、关于出口前准备贸易企业所需的资质和材料
国内出口贸易企业需具备的资质和材料:
一、中国海关要求提供:
医疗器械注册证(非医用则不需要)
二、国外客户可能要求提供(具体以国外进口商或者目的国家的要求为准,中国海关不收取,申报时也无需随附):
1.营业执照(经营范围有相关经营内容)。
2.企业生产许可证(生产企业)。
3.产品检验报告(生产企业)。
4.产品说明书(跟着产品提供)、标签(随附产品提供)。
5.产品批次/号(外包装)。
6.产品质量安全书或合格证(跟着产品提供)。
7.产品样品图片及外包装图片。
3、关于医疗器械经营资质
海关无医疗器械经营资质要求,进行出口申报时无须随附。
4、关于检测试剂归类
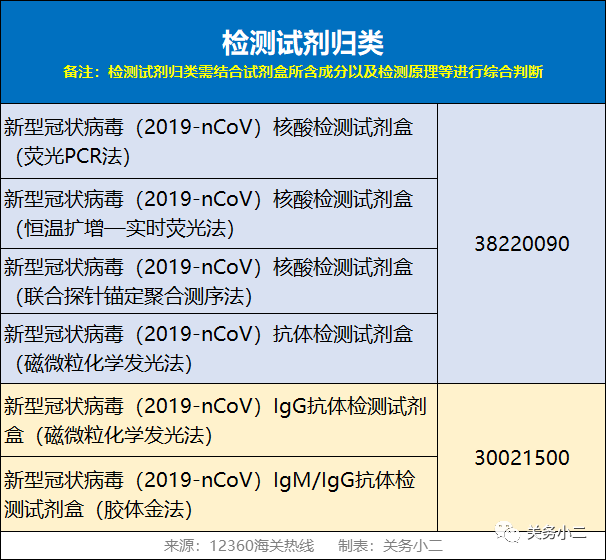
常见的新型冠状病毒(2019-nCoV)核酸检测试剂盒(荧光PCR法)、新型冠状病毒(2019-nCoV)核酸检测试剂盒(恒温扩增—实时荧光法)、新型冠状病毒(2019-nCoV)核酸检测试剂盒(联合探针锚定聚合测序法)和新型冠状病毒(2019-nCoV)抗体检测试剂盒(磁微粒化学发光法)归入38220090;
新型冠状病毒(2019-nCoV)IgG抗体检测试剂盒(磁微粒化学发光法)、新型冠状病毒(2019-nCoV)IgM/IgG抗体检测试剂盒(胶体金法)归入30021500。
新型冠状病毒检测试剂盒的检测方法较多,且新方法在不断出现,其归类需要结合试剂盒所含成分以及检测原理等进行综合判断。
各进出口企业在参考上述税号时,请勿仅凭借试剂盒品名判断,还要结合上述商品的成分和检测原理进行对应。
5、关于美国放宽防护物资准入的更新
3月28日,美国食品药品监督管理局(FDA)对口罩相关的紧急使用授权(EUA)范围作出如下解释,本次授权对象仅限于下表所列产品,以及经授权方式净化达到下表条件的产品,以在新冠疫情爆发且相关物资短缺的情况下,将其作为美国疾病控制与预防中心(CDC)的推荐产品,供医疗人员使用以避免接触经空气传播的致病微粒。